Introduzione
Le chiamate al centro di farmacologia dell’allattamento della Texas Tech University che riguardavano il semaglutide sono aumentate di oltre il 500% tra il 2021 e il 2024 (Diab et al., 2024). È un indicatore concreto di una domanda reale: molte donne che allattano e desiderano gestire il peso si chiedono se possano usare questi farmaci, e i loro medici si trovano spesso senza una risposta basata su dati.
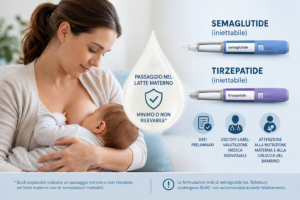
Il punto di partenza è che le schede tecniche di semaglutide e tirzepatide ne raccomandano la sospensione durante l’allattamento, non perché esista una tossicità dimostrata, ma perché al momento dell’autorizzazione mancavano studi specifici. Negli ultimi due anni qualche dato è arrivato. Ma cosa mostrano realmente?
Cos’è la dose relativa per il lattante
Per valutare se un farmaco assunto dalla madre sia un problema per il bambino allattato, la farmacologia dell’allattamento usa un parametro chiamato RID (dose relativa per il lattante): è la quantità di farmaco che il bambino riceve attraverso il latte, espressa come percentuale della dose materna rapportata al peso. Per convenzione, un RID inferiore al 10% è considerato generalmente compatibile con l’allattamento per la maggior parte dei farmaci.
Il RID, però, racconta solo una parte della storia: misura il trasferimento diretto del farmaco. Non dice nulla sugli effetti indiretti che un farmaco dimagrante può avere sulla produzione e sulla composizione del latte. Su questo punto si torna più avanti.
Il problema dei farmaci dimagranti in allattamento non è tanto quanto farmaco arriva al bambino, ma quanto la rapida perdita di peso della madre può incidere sulla qualità della sua alimentazione e del suo latte.
Semaglutide iniettabile: cosa mostra lo studio sul latte materno
Lo studio più informativo sul semaglutide è quello di Diab e colleghi, pubblicato su Nutrients nel 2024 (Diab et al., 2024). Otto madri che allattavano, in trattamento con semaglutide sottocutaneo a dosi settimanali comprese tra 0,25 e 1 mg, hanno donato campioni di latte raccolti a 0, 12 e 24 ore dalla somministrazione. In nessun campione il semaglutide è risultato rilevabile, con un limite di rilevazione del metodo di 1,7 mcg/L.
Poiché il farmaco non era misurabile, gli autori hanno calcolato uno scenario peggiore, ipotizzando che il latte contenesse semaglutide alla soglia inferiore di quantificazione del metodo. Anche in questa ipotesi prudenziale, la dose relativa per il lattante risultava in media dell’1,12%, con un valore massimo aggiustato dell’1,26%: molto al di sotto della soglia convenzionale del 10%. Le madri hanno riferito che i lattanti — di età compresa tra 7 e 23 mesi — mostravano crescita e sviluppo regolari.
A questo si aggiunge un dato farmacologico noto: il semaglutide è una molecola che, assunta per bocca, viene assorbita pochissimo (biodisponibilità orale inferiore all’1% negli adulti). Anche l’eventuale piccola quota presente nel latte avrebbe quindi scarse probabilità di essere assorbita dall’intestino del lattante (LactMed, 2024).
La questione delle formulazioni orali: il caso del SNAC
Esiste però una distinzione importante. Alcune formulazioni orali di semaglutide — in Italia il Rybelsus — contengono il salcaprozato sodico (SNAC), un eccipiente che funziona da potenziatore dell’assorbimento: serve proprio a far passare nel sangue una molecola che da sola non verrebbe assorbita.
Il timore, segnalato dai database di farmacologia dell’allattamento, è che il SNAC possa trasferirsi nel latte e accumularsi nel lattante (LactMed, 2024). Non esistono dati diretti che quantifichino questo rischio, ma il principio di precauzione porta a una raccomandazione netta: durante l’allattamento, se si usa il semaglutide, va usata esclusivamente la forma iniettabile, mai quella orale.
Tirzepatide: dati preliminari e dato regolatorio
Sul tirzepatide la situazione è in evoluzione. Fino al 2024 non esistevano dati clinici; oggi ne esistono due, entrambi da considerare con le loro cautele.
Lo studio osservazionale (preliminare)
Uno studio condotto dallo stesso gruppo che ha studiato il semaglutide ha analizzato il latte di cinque donne che assumevano tirzepatide sottocutaneo a dosi di 2,5–5 mg a settimana, con campioni raccolti fino a 168 ore dopo la dose (Thompson et al., 2025). Il tirzepatide non è risultato quantificabile in alcun campione, e la dose relativa stimata per il lattante era inferiore allo 0,05%. È un risultato rassicurante, ma va letto con una qualifica precisa: si tratta di un preprint, cioè di un lavoro non ancora sottoposto a revisione tra pari, i cui dati potrebbero cambiare nella pubblicazione definitiva.
Il dato del produttore
La scheda tecnica statunitense del tirzepatide riporta uno studio dell’azienda produttrice su 11 donne che allattavano, alle quali è stata somministrata una singola dose da 5 mg. Il tirzepatide è risultato non rilevabile (limite 4 mcg/L) in 164 campioni su 171; nei 7 campioni rimanenti la quantità cumulativa corrispondeva a meno dello 0,02% della dose materna (FDA, 2025). Anche questo dato ha un limite metodologico esplicito: una dose singola raggiunge solo circa metà delle concentrazioni che si avrebbero con l’uso continuativo, quindi le quantità nel latte durante un trattamento reale sono presumibilmente superiori a quelle misurate.
Sul piano farmacologico vale per il tirzepatide lo stesso ragionamento del semaglutide, anzi rafforzato: è una grande molecola peptidica (peso molecolare di circa 4800 Da), poco propensa a passare nel latte e con scarsa probabilità di essere assorbita dall’intestino del lattante, dove viene in buona parte degradata (LactMed, 2026). Sintetizzando i due dati, il database istituzionale LactMed nella revisione di febbraio 2026 afferma che il tirzepatide è in genere indetectabile nel latte a dosi fino a 5 mg e che, se una madre necessita del farmaco, questo non costituisce di per sé una ragione per interrompere l’allattamento — pur raccomandando cautela, in particolare con neonati o prematuri (LactMed, 2026).
Oltre il passaggio nel latte: nutrizione materna e composizione del latte
Concentrarsi solo sul trasferimento diretto del farmaco rischia di far perdere di vista il punto clinicamente più rilevante. Semaglutide e tirzepatide agiscono riducendo l’introito calorico, e in allattamento questo solleva una questione di nutrizione.
È una distinzione che cambia il modo di impostare la decisione clinica: la domanda non è solo “il farmaco arriva al bambino?”, ma anche “questa madre, con questo farmaco, riesce a mantenere un’alimentazione adeguata per sé e per la produzione di latte?”. La risposta dipende dal singolo caso e va monitorata nel tempo, sulla crescita del lattante e sullo stato nutrizionale della madre.
Cosa significa nella pratica clinica
Da quanto sopra discendono alcuni punti fermi. Il primo è di natura regolatoria: l’uso di semaglutide e tirzepatide durante l’allattamento è fuori indicazione rispetto alle schede tecniche autorizzate, che ne raccomandano la sospensione. Questo non significa che sia vietato, ma che si tratta di una scelta off-label, che va condivisa con il medico, motivata clinicamente e accompagnata da un consenso informato consapevole.
Il secondo è che la decisione non può essere generica: dipende dall’indicazione (un conto è il diabete, un conto la sola gestione del peso), dall’età del lattante (con un neonato o un prematuro la cautela è maggiore), dalla possibilità di un monitoraggio adeguato. Il terzo è che, qualunque sia la scelta, una donna che allatta non dovrebbe mai iniziare, sospendere o modificare in autonomia una terapia con questi farmaci sulla base di informazioni reperite online.
Conclusioni
Le evidenze accumulate negli ultimi due anni hanno spostato il quadro da “nessun dato” a “dati preliminari rassicuranti sul trasferimento”. Il semaglutide iniettabile non è risultato rilevabile nel latte materno e i lattanti esposti non hanno mostrato effetti avversi; per il tirzepatide due fonti indipendenti — uno studio preliminare e il dato del produttore — convergono nell’indicare un passaggio nel latte trascurabile, pur con i limiti metodologici di entrambe. Le formulazioni orali di semaglutide restano sconsigliate per la presenza del SNAC.
Resta aperta la questione degli effetti indiretti del dimagrimento sulla nutrizione materna e sul latte, che nessuno degli studi disponibili ha ancora affrontato e che rappresenta oggi l’area di maggiore incertezza.
In sintesi: i dati attuali indicano che semaglutide e tirzepatide iniettabili passano nel latte materno in quantità minime o non rilevabili, ben sotto le soglie di sicurezza convenzionali; resta tuttavia un uso off-label, da decidere con il medico caso per caso, tenendo conto non solo del farmaco ma anche dell’impatto del calo di peso sull’alimentazione della madre.
Domande frequenti
Posso continuare ad allattare se prendo Ozempic o Wegovy?
I dati disponibili indicano che il semaglutide iniettabile non è rilevabile nel latte materno e che i lattanti esposti non hanno mostrato effetti avversi. Si tratta però di un uso fuori indicazione: la decisione va presa insieme al medico curante, non in autonomia.
Il Rybelsus (semaglutide in compresse) è equivalente all’iniezione per chi allatta?
No. Le compresse contengono il salcaprozato sodico (SNAC), un potenziatore di assorbimento che potrebbe passare nel latte e accumularsi nel lattante. Durante l’allattamento, se si usa il semaglutide, va usata solo la forma iniettabile.
E il Mounjaro (tirzepatide)?
I dati sono più recenti e ancora preliminari, ma uno studio osservazionale e il dato del produttore concordano nell’indicare un passaggio nel latte trascurabile. La cautela raccomandata è maggiore con neonati o bambini nati prematuri.
Questi farmaci possono far diminuire il latte?
Non esistono studi che lo dimostrino, ma è una possibilità teorica concreta: riducendo l’appetito e favorendo un calo di peso rapido, possono incidere sull’alimentazione della madre e quindi sulla produzione di latte. È l’aspetto che richiede più attenzione e monitoraggio.
Devo aspettare un certo tempo dopo il parto prima di iniziare?
La produzione di latte si stabilizza nelle prime settimane dopo il parto. Avviare un farmaco che riduce l’appetito e induce calo di peso in questa fase delicata richiede particolare prudenza: i tempi vanno discussi con il medico, valutando priorità nutrizionali e obiettivi di allattamento.
Se ho preso il farmaco senza sapere di allattare devo preoccuparmi?
I dati disponibili sono rassicuranti sul trasferimento del farmaco nel latte. È comunque opportuno informare il medico, che potrà valutare la situazione specifica e l’eventuale monitoraggio della crescita del bambino.
Glossario dei termini principali
GLP-1 AR: agonisti recettoriali del GLP-1, la classe di farmaci a cui appartiene il semaglutide. Il tirzepatide agisce su due recettori (GLP-1 e GIP) e viene talvolta indicato come doppio agonista.
RID (dose relativa per il lattante): quantità di farmaco che il bambino allattato riceve attraverso il latte, espressa come percentuale della dose materna corretta per il peso. Un valore inferiore al 10% è generalmente considerato compatibile con l’allattamento.
SNAC (salcaprozato sodico): eccipiente presente in alcune formulazioni orali di semaglutide; agisce da potenziatore dell’assorbimento intestinale del farmaco.
Biodisponibilità orale: frazione di un farmaco assunto per bocca che raggiunge effettivamente la circolazione sanguigna. Per semaglutide e tirzepatide è molto bassa, ed è il motivo per cui vengono somministrati per iniezione.
Preprint: versione di uno studio resa pubblica prima della revisione tra pari (peer review). I dati sono provvisori e possono cambiare nella pubblicazione definitiva su rivista.
Uso off-label: impiego di un farmaco al di fuori delle indicazioni, delle dosi o delle popolazioni previste dalla scheda tecnica autorizzata. È una pratica legittima quando clinicamente motivata e documentata.
Bibliografia
- Diab H, Fuquay T, Datta P, Bickel U, Thompson J, Krutsch K. (2024)
- Subcutaneous Semaglutide during Breastfeeding: Infant Safety Regarding Drug Transfer into Human Milk. Nutrients. 16(17):2886.
https://doi.org/10.3390/nu16172886 - Drugs and Lactation Database (LactMed®). (2024)
- Semaglutide. Bethesda (MD): National Institute of Child Health and Human Development. Ultima revisione 15 dicembre 2024.
https://www.ncbi.nlm.nih.gov/books/NBK500980/ - Drugs and Lactation Database (LactMed®). (2026)
- Tirzepatide. Bethesda (MD): National Institute of Child Health and Human Development. Ultima revisione 15 febbraio 2026.
https://www.ncbi.nlm.nih.gov/books/NBK581488/ - Thompson J, Diab H, Datta P, Krutsch K. (2025)
- Tirzepatide (Zepbound) in Human Milk During Periods of Maternal Dosing. SSRN. [Preprint — non ancora sottoposto a revisione tra pari]
https://doi.org/10.2139/ssrn.5387250 - U.S. Food and Drug Administration. (2025)
- Mounjaro (tirzepatide) — Prescribing Information, sezione Lactation. FDA.
https://www.accessdata.fda.gov/drugsatfda_docs/label/2025/217806s031lbl.pdf
