Introduzione
Per oltre un decennio, tutti i farmaci realmente efficaci contro l’obesità hanno avuto una caratteristica comune: si somministravano per iniezione. Liraglutide, semaglutide, tirzepatide — la classe degli agonisti recettoriali del GLP-1 (GLP-1 AR) ha cambiato il trattamento dell’obesità, ma ha continuato a chiedere al paziente di fare un’iniezione ogni settimana. Molti hanno rinunciato prima di provare, per paura dell’ago o per la difficoltà di gestire una terapia refrigerata.
Dal dicembre 2025 qualcosa è cambiato e la pillola contro l’obesità è oggi realtà negli USA. La Food and Drug Administration statunitense ha approvato la prima pillola GLP-1 AR specificamente indicata per l’obesità: il semaglutide orale 25 mg di Novo Nordisk. Quattro mesi dopo, nell’aprile 2026, si è aggiunta una seconda pillola di una classe tecnologicamente diversa: l’orforglipron di Eli Lilly. In Italia nessuna delle due è ancora arrivata.
Ma cosa dicono realmente i dati scientifici disponibili, e cosa cambia davvero per chi oggi aspetta la pillola?
Perché è stata così difficile da realizzare la pillola contro l’obesità
Il GLP-1 (glucagon-like peptide-1) è un ormone naturalmente prodotto dall’intestino dopo i pasti. I farmaci GLP-1 AR ne imitano l’azione, riducendo appetito e apporto calorico. Il problema è che il GLP-1 è una piccola proteina, e come tutte le proteine viene degradato dall’acido gastrico e dagli enzimi digestivi prima di poter essere assorbito. Per vent’anni questo ha obbligato la classe a rimanere iniettiva.
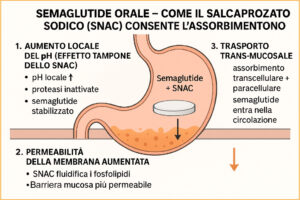
Le due pillole oggi approvate negli Stati Uniti hanno risolto il problema in due modi completamente diversi. Il semaglutide orale trasporta la stessa molecola del farmaco iniettabile attraverso la parete dello stomaco grazie a un eccipiente speciale chiamato SNAC (sale dell’acido salcaprozato), che aumenta temporaneamente il pH locale e facilita il passaggio transcellulare.
L’orforglipron invece non è una proteina: è una piccola molecola chimica progettata da zero, non peptidica, che attiva lo stesso recettore del GLP-1 ma resiste naturalmente all’acido gastrico e non richiede tecnologie di assorbimento. Due strade per la stessa destinazione.
Per la prima volta, una terapia efficace per l’obesità si assume come una qualsiasi compressa.
Il semaglutide orale c’era già: la storia di Rybelsus
La prima pillola di semaglutide, nata per il diabete
Il semaglutide orale non è una novità assoluta. Dal 2019 (FDA) e 2020 (EMA) è in commercio con il nome di Rybelsus, indicato per il trattamento del diabete di tipo 2 alle dosi di 3, 7 e 14 mg. Molti pazienti con obesità lo hanno ricevuto off-label per il calo ponderale, a volte, con risultati modesti perché la dose registrata per il diabete era semplicemente troppo bassa per riprodurre l’effetto ponderale del semaglutide 2,4 mg sottocutaneo.
La formulazione migliorata del 2025
Nel 2025 Novo Nordisk ha introdotto una nuova formulazione di Rybelsus, denominata tecnicamente R2, con eccipienti modificati che raddoppiano la biodisponibilità — dall’intervallo 0,4–1% della formulazione originale all’1–2% della nuova (FDA, 2025). La conseguenza pratica è che la nuova formulazione consente di ottenere la stessa esposizione sistemica con dosi inferiori: sono arrivate le nuove compresse da 1,5, 4 e 9 mg (di forma tonda, anziché ovale come le precedenti), che hanno sostituito rispettivamente le vecchie da 3, 7 e 14 mg. In Italia la nuova formulazione è già disponibile da mesi e i pazienti in terapia sono stati transitati alla dose equivalente.
La novità tecnicamente rilevante è che la stessa piattaforma formulativa è stata estesa al dosaggio di 25 mg studiato specificamente per l’obesità. Il semaglutide orale 25 mg — commercializzato negli USA come Wegovy pill — contiene esattamente gli stessi eccipienti (semaglutide, stearato di magnesio, SNAC) della nuova Rybelsus, con un quarto strength aggiunto per la titolazione all’indicazione ponderale. Non è quindi un semplice “Rybelsus ad alta dose”: è la formulazione migliorata, portata fino alla dose effettivamente necessaria a trattare l’obesità.
Semaglutide orale 25 mg: cosa dice OASIS 4
L’approvazione statunitense si basa sullo studio OASIS 4 (Wharton et al., 2025), un trial di fase 3 condotto in 307 adulti senza diabete, con obesità (BMI ≥30) oppure sovrappeso (BMI ≥27) associato ad almeno una complicanza, trattati per 64 settimane con semaglutide orale 25 mg una volta al giorno oppure placebo, insieme a counselling sullo stile di vita basato su un deficit calorico di 500 kcal al giorno.
I risultati possono essere letti con due diverse lenti statistiche. Se si considerano tutti i pazienti randomizzati, compresi quelli che hanno interrotto la terapia (la misura più vicina alla realtà clinica), la perdita di peso media è stata del 13,6% a 64 settimane, contro il 2,2% del placebo. Se si considerano solo i pazienti che hanno completato la terapia come previsto (la misura dell’effetto massimo), il calo è stato del 16,6%. Quasi il 30% dei pazienti trattati ha avuto una perdita di peso del 20% o più (29,7% vs 3,3% nel placebo), e la metà ha superato la soglia del 15%. Il 71,1% dei pazienti con prediabete al basale è tornato alla normoglicemia (contro il 33,3% nel gruppo placebo). Gli effetti indesiderati gravi sono stati meno frequenti con semaglutide (3,9%) che con il placebo (8,8%); gli effetti gastrointestinali — nausea, vomito, diarrea — si sono presentati nel 74% dei pazienti trattati, in linea con il profilo già noto della forma iniettabile, in forma per lo più lieve-moderata.
Come si prende
La compressa richiede una regola scomoda ma non negoziabile, perché l’assorbimento mediato da SNAC dipende da condizioni gastriche molto specifiche: va assunta al mattino a stomaco vuoto, con un sorso d’acqua (non più di 120 mL), e bisogna attendere almeno 30 minuti (io consiglio 60 minuti) prima di mangiare, bere altro o assumere qualsiasi altro farmaco. Cibo, altre bevande e altri medicinali riducono in modo significativo la quantità di semaglutide che raggiunge il sangue. Per molti pazienti questo diventa una routine mattutina (sveglia, pillola, doccia, colazione); per altri è un ostacolo serio all’aderenza. Il label statunitense segnala inoltre che le concentrazioni plasmatiche ottenute con la pillola sono mediamente più basse e con maggiore variabilità rispetto all’iniezione: una quota di pazienti potrebbe quindi non raggiungere livelli terapeutici sufficienti, ed è ragionevole in questi casi considerare il passaggio alla forma iniettabile.
Orforglipron: l’altra pillola, diversa nella sostanza
Orforglipron è stato approvato dalla FDA il 1° aprile 2026 con il nome commerciale statunitense di Foundayo, e commercializzato dal 6 aprile. Si tratta di una piccola molecola non peptidica — un farmaco chimico, non una proteina — che attiva direttamente il recettore del GLP-1 senza aver bisogno di alcun enhancer di assorbimento. La conseguenza pratica più importante per il paziente è che può essere assunto in qualsiasi momento della giornata, con o senza cibo, con qualsiasi quantità d’acqua, senza attese e senza incompatibilità con altri farmaci assunti a stomaco vuoto. Una caratteristica già presentata in dettaglio in un precedente articolo pubblicato su obesita.com, quando il farmaco era ancora in sviluppo clinico.
Cosa dice ATTAIN-1
I dati di efficacia pubblicati poco dopo l’approvazione sul New England Journal of Medicine (Wharton et al., 2025) vengono dal trial ATTAIN-1, condotto in 3127 pazienti adulti con obesità senza diabete, trattati per 72 settimane. Alla dose massima commerciale di 17,2 mg al giorno, orforglipron ha prodotto una perdita di peso media dell’11,2% a 72 settimane, contro il 2,1% del placebo. Il 54,6% dei pazienti ha superato la soglia del 10% di calo, il 36,0% quella del 15%, il 18,4% quella del 20%. Analogamente al semaglutide, si è osservato un marcato miglioramento dei fattori di rischio cardiometabolico: riduzione di pressione arteriosa, trigliceridi, colesterolo non-HDL, e ritorno alla normoglicemia in una percentuale tra il 74,6% e l’83,7% dei pazienti con prediabete al basale.
Un dato particolarmente utile per rispondere a una domanda frequente viene dall’analisi con DXA (densitometria a raggi X a doppia energia) condotta su un sottogruppo: della perdita di peso totale, il 73,1% è risultato grasso corporeo e il 26,9% massa magra, con una riduzione del grasso viscerale del 19%. Proporzioni in linea con quanto osservato con altri GLP-1 AR, che smentiscono l’idea che la pillola faccia “perdere soprattutto muscolo”. Gli effetti indesiderati sono stati prevalentemente gastrointestinali, sovrapponibili per tipo a quelli degli altri farmaci della classe, generalmente lievi-moderati, più frequenti nelle prime settimane durante la titolazione.
Dall’iniezione alla pillola contro l’obesità: ATTAIN-MAINTAIN
Una domanda che molti pazienti già in terapia iniettabile si pongono è se la pillola contro l’obesità potrà un giorno sostituire l’iniezione senza perdere il peso raggiunto. A questa domanda risponde ATTAIN-MAINTAIN, un trial di fase 3 di 52 settimane condotto su 376 pazienti che avevano già raggiunto un plateau ponderale con semaglutide 2,4 mg o tirzepatide 10–15 mg, e sono stati poi ri-randomizzati a orforglipron orale oppure a placebo. I dati topline, comunicati da Lilly nel dicembre 2025 e in attesa di pubblicazione peer-reviewed, mostrano che l’endpoint primario è stato raggiunto. A 24 settimane dal cambio di terapia, i pazienti passati a orforglipron hanno sostanzialmente mantenuto il peso perso (variazione media di −0,1 kg nel braccio ex-semaglutide e +2,6 kg in quello ex-tirzepatide), mentre chi è passato a placebo ha recuperato oltre 9 kg in entrambi i bracci. A 52 settimane, la differenza rispetto al peso pre-switch restava contenuta: circa 1 kg per gli ex-semaglutide, 5 kg per gli ex-tirzepatide. È il primo trial formale di switch iniettabile → orale nella classe, e conferma due cose insieme: che il passaggio alla pillola è praticabile senza sacrificare i risultati raggiunti, e che la terapia farmacologica dell’obesità è per sua natura cronica, perché senza il farmaco il peso torna rapidamente.
Quando arrivEranno in Italia lE pillolE contro l’obesità
Quando arriverà in Italia la pillola contro l’obesità? Il dossier di registrazione del semaglutide orale 25 mg per l’obesità è stato sottomesso all’Agenzia Europea del Farmaco (EMA) nella seconda metà del 2025 e le discussioni in comitato scientifico (CHMP) sono attive da febbraio 2026. Nei tempi standard di una procedura europea, una decisione della Commissione è attesa nel corso del 2026, cui seguirà l’iter italiano presso AIFA per l’immissione in commercio e la definizione della rimborsabilità. L’arrivo effettivo in farmacia in Italia è quindi plausibile verso la fine del 2026/inizio 2027, fermo restando che il calendario esatto dipende dalle decisioni regolatorie in corso.
Per orforglipron le tempistiche europee sono più indietro: la sottomissione al dossier EMA non è ancora stata confermata pubblicamente alla data odierna, e realisticamente la disponibilità italiana non è collocabile prima del primo quadrimestre 2027. Va ricordato che l’arrivo in commercio europeo non significa automaticamente rimborsabilità a carico del Servizio Sanitario Nazionale: come avvenuto per la forma iniettabile di semaglutide e per tirzepatide, è probabile che in una prima fase il farmaco sia accessibile solo con prescrizione a carico diretto del paziente.
Cosa sta arrivando dietro l’angolo
Le due pillole contro l’obesità sono il primo fronte di un’ondata più ampia. Il farmaco oggi più atteso è il retatrutide, un agonista che agisce contemporaneamente su tre recettori ormonali (GIP, GLP-1 e glucagone) e che nel primo studio di fase 3 pubblicato — TRIUMPH-4, dati topline di dicembre 2025 ancora in attesa di pubblicazione peer-reviewed — ha fatto registrare una perdita di peso media del 28,7% a 68 settimane, la più alta mai ottenuta in un trial registrativo per l’obesità (Lilly, 2025). Sono attesi nel corso del 2026 altri sette readout dello stesso programma; l’approvazione, se tutto procederà, è realisticamente collocabile nel 2027–2028.
Sul fronte Novo Nordisk, altre due molecole sono in avanzata fase di sviluppo: CagriSema, combinazione iniettabile settimanale di semaglutide e di cagrilintide (un analogo dell’amilina, ormone della sazietà periferica), e amycretin, una nuova molecola entrata in fase 3 a inizio 2026 sia in formulazione iniettabile sia orale. L’obesità sta passando, in pochi anni, da un’area farmacologicamente povera a una delle più affollate della medicina moderna.
Conclusioni
La pillola contro l’obesità GLP-1 AR, non è la versione “minore” dell’iniezione. Nei trial registrativi, il semaglutide orale 25 mg ha prodotto una perdita di peso sostanzialmente sovrapponibile a quella della forma iniettabile 2,4 mg. Orforglipron, con un meccanismo di assorbimento completamente diverso e senza vincoli di assunzione, offre un’efficacia leggermente inferiore in termini assoluti ma con un profilo d’uso più semplice nella vita quotidiana. Entrambi, pur con differenze, rappresentano un cambio di paradigma reale: per la prima volta chi rifiuta l’iniezione non è costretto a rinunciare a una terapia efficace.
Per il paziente italiano che oggi si chiede se valga la pena aspettare, la risposta onesta è che l’attesa sarà misurata in mesi, non più in anni, e che il calendario sarà definito dalle prossime decisioni regolatorie europee.
In sintesi: la prima pillola contro l’obesità è una realtà approvata negli Stati Uniti e in Italia arriverà verosimilmente tra fine 2026/inizio 2027 (semaglutide orale) e primo quadrimestre 2027 (orforglipron); nel frattempo, i farmaci iniettabili oggi disponibili restano la scelta ottimale per chi può iniziare subito, mentre la pipeline in arrivo promette ulteriori miglioramenti di efficacia.
Domande frequenti (FAQ)
Posso già farmela prescrivere dall’estero o procurarmela online?
Nessuna delle pillole contro l’obesità (semaglutide orale 25 mg e orforglipron) è attualmente autorizzata in Italia o in Europa: acquistarle all’estero o da farmacie online espone a rischi concreti (prodotti contraffatti, assenza di supervisione clinica, mancanza di copertura per eventi avversi). La scelta prudente è attendere l’approvazione regolatoria europea o, se il trattamento è clinicamente indicato e urgente, avviare una terapia con le formulazioni iniettabili già disponibili e rimborsate in specifici contesti.
Se sono già in terapia con iniezione, mi conviene passare alla pillola quando arriverà?
Non necessariamente. Per chi ha raggiunto buoni risultati con la forma iniettabile, passare alla pillola significa affrontare i vincoli di assunzione a digiuno (nel caso di semaglutide) e una variabilità di assorbimento potenzialmente maggiore. Il label statunitense prevede esplicitamente la possibilità di switch in entrambe le direzioni con dosi equivalenti definite (semaglutide 2,4 mg iniettabile ↔ 25 mg orale): la decisione va discussa caso per caso, considerando preferenze del paziente, aderenza e risposta individuale.
La pillola contro l’obesità dà meno effetti collaterali dell’iniezione?
No, non in modo clinicamente rilevante. Il profilo di effetti indesiderati — soprattutto gastrointestinali — è sostanzialmente sovrapponibile tra pillola e iniezione per semaglutide, e analogo per orforglipron. La frequenza di nausea, vomito e diarrea dipende più dalla velocità di titolazione che dalla via di somministrazione.
Come si sceglierà tra semaglutide orale e orforglipron?
Oggi non ci sono studi testa-a-testa e ogni confronto numerico tra i due farmaci va preso con cautela. Nei rispettivi trial, semaglutide orale 25 mg ha mostrato un’efficacia leggermente superiore in termini assoluti, ma con vincoli stringenti di assunzione; orforglipron ha un’efficacia leggermente inferiore ma si prende senza restrizioni. La scelta sarà probabilmente guidata dal profilo individuale: chi riesce a tenere una routine mattutina stabile potrà preferire semaglutide; chi ha orari irregolari, viaggia spesso o assume altri farmaci a stomaco vuoto troverà orforglipron più compatibile con la propria vita.
Il costo sarà simile a quello delle iniezioni?
Le informazioni disponibili dagli Stati Uniti suggeriscono che il prezzo di partenza della pillola sarà verosimilmente inferiore a quello dell’iniettabile, grazie ai minori costi di produzione (soprattutto nel caso di orforglipron, che è una molecola chimica sintetizzabile con processi industriali standard, non una proteina da fermentazione). In Italia il prezzo finale dipenderà però dalla negoziazione AIFA e dalla eventuale rimborsabilità, variabili oggi non prevedibili.
Glossario dei termini principali
GLP-1 AR (agonisti recettoriali del GLP-1). Classe di farmaci che imitano l’azione del glucagon-like peptide-1, ormone intestinale coinvolto nella regolazione dell’appetito e della glicemia. Includono semaglutide, liraglutide, dulaglutide e, come nuova generazione non peptidica, orforglipron.
Biodisponibilità orale. Percentuale della dose somministrata per bocca che raggiunge effettivamente il sangue. Per i peptidi è tipicamente molto bassa senza tecnologie dedicate; il semaglutide orale raggiunge l’1–2% grazie all’eccipiente SNAC.
SNAC (sale dell’acido salcaprozato). Eccipiente che, co-formulato con il semaglutide, aumenta localmente il pH gastrico e facilita l’attraversamento della parete dello stomaco da parte della molecola. È il meccanismo su cui si regge l’assorbimento del semaglutide orale.
Piccola molecola non peptidica. Farmaco di sintesi chimica, diverso dai peptidi (cioè dalle proteine): orforglipron ne è un esempio. A differenza dei peptidi, resiste naturalmente all’acido gastrico e può essere prodotto con processi industriali più semplici e meno costosi.
CHMP / EMA / AIFA. Il Committee for Medicinal Products for Human Use è il comitato scientifico dell’Agenzia Europea del Farmaco (EMA) che esprime il parere tecnico sull’autorizzazione; la Commissione europea formalizza poi la decisione. L’Agenzia Italiana del Farmaco (AIFA) gestisce l’immissione in commercio e la rimborsabilità a livello nazionale.
Trial-product estimand e treatment-policy estimand. Due modi diversi di analizzare gli stessi dati di un trial: il primo stima l’effetto come se tutti i pazienti avessero aderito alla terapia (misura dell’efficacia massima), il secondo considera tutti i pazienti randomizzati compresi quelli che hanno sospeso (misura più vicina alla pratica clinica).
Bibliografia
- Eli Lilly and Company (2025)
- ATTAIN-MAINTAIN — Topline results for orforglipron as oral maintenance therapy following injectable incretin-based treatment. Press release, 18 December 2025. Peer-reviewed publication expected 2026.
- Food and Drug Administration (2025)
- Rybelsus® (semaglutide) tablets — Highlights of prescribing information. Reference ID 5679328.
https://www.accessdata.fda.gov/drugsatfda_docs/label/2025/213051s024,s028s029lbl.pdf - Food and Drug Administration (2025)
- Wegovy® (semaglutide) tablets — Highlights of prescribing information. NDA 218316.
https://www.accessdata.fda.gov/drugsatfda_docs/label/2025/218316Orig1s000lbl.pdf - Food and Drug Administration (2026)
- Foundayo™ (orforglipron) tablets — Highlights of prescribing information. Eli Lilly and Company, April 2026.
- Knop FK, Aroda VR, do Vale RD, et al. (2023)
- Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 402(10403):705–719.
https://doi.org/10.1016/S0140-6736(23)01185-6 - Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. (2023)
- Semaglutide and cardiovascular outcomes in obesity without diabetes. N Engl J Med. 389(24):2221–2232.
https://doi.org/10.1056/NEJMoa2307563 - Novo Nordisk (2025)
- FDA approval for Wegovy® pill (once-daily oral semaglutide 25 mg) — Company announcement, 22 December 2025.
- Wharton S, Aronne LJ, Stefanski A, et al. (2025)
- Orforglipron, an Oral Small-Molecule GLP-1 Receptor Agonist for Obesity Treatment. N Engl J Med. 393(18):1796–1806.
https://doi.org/10.1056/NEJMoa2511774 - Wharton S, Lingvay I, Bogdanski P, et al. (2025)
- Oral Semaglutide at a Dose of 25 mg in Adults with Overweight or Obesity. N Engl J Med. 393(11):1077–1087.
https://doi.org/10.1056/NEJMoa2500969
