Introduzione
Quando nel settembre 2025 lo studio STEP UP ha riportato che quasi uno su quattro pazienti trattati con semaglutide 7,2 mg aveva sviluppato fenomeni di disestesia (caratterizzata da bruciore e formicolio cutaneo), molti clinici si sono chiesti: è un segnale nuovo o qualcosa che abbiamo sempre visto senza riconoscerlo? La risposta, a leggere con attenzione la letteratura degli ultimi tre anni, è che il fenomeno era già presente — nei foglietti illustrativi dei GLP1, in case report isolati, nei database di farmacovigilanza — ma non aveva ancora ricevuto un nome preciso né una narrazione organica (Burke et al., 2025; Stokes et al., 2025).
La disestesia non è un dettaglio marginale: con semaglutide 7,2 mg è il secondo evento avverso per frequenza dopo i disturbi gastrointestinali, ed è stato riportato in misura variabile con tutti i principali farmaci della classe incretino-mimetica, inclusi tirzepatide e semaglutide orale. Capirne l’incidenza reale, il pattern temporale e il meccanismo probabile non è un esercizio accademico, ma uno strumento pratico per gestirla meglio — sia per il paziente che la vive, sia per il medico che deve decidere se interrompere, ridurre la dose o proseguire.
Ma cosa sappiamo davvero di questa sensazione che brucia, formica e turba senza lasciare segni visibili sulla cute?
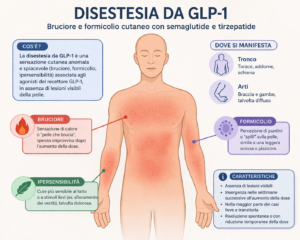
Cos’è la disestesia e come si manifesta
Con il termine disestesia (dal greco dys, alterato, e aísthēsis, sensazione) si indica qualsiasi percezione cutanea anomala e spiacevole — bruciore, formicolio, ipersensibilità anche al minimo sfioramento, sensazione di prurito profondo o dolore cutaneo — non associata a lesioni visibili della pelle. È una categoria ampia che include: allodinia (dolore evocato da stimoli normalmente non dolorosi, come il contatto con un tessuto), iperestesia (aumento abnorme della sensibilità tattile), parestesia (formicolio o torpore) e sensibilizzazione cutanea diffusa.
Nel contesto degli studi sui GLP-1 AR, la disestesia si manifesta tipicamente come una sensazione di bruciore o di “pelle viva” distribuita sul tronco o sugli arti, talvolta associata a prurito o a una vaga dolorabilità superficiale. I partecipanti allo studio STEP UP che l’hanno segnalata descrivono una sintomatologia nel complesso coerente, di intensità lieve nella grande maggioranza dei casi, con esordio acuto nei giorni o nelle settimane successive all’aumento della dose (Wharton et al., 2025). Non sono stati riportati eventi gravi. Nella classificazione usata in STEP UP, la categoria “disestesia” comprendeva allodinia, sensazione di bruciore, iperestesia, dolore cutaneo, parestesia, pelle sensibile, sensazione di bruciore cutaneo, fastidio cutaneo e sensibilizzazione cutanea — un insieme eterogeneo accomunato dall’anomalia percettiva in assenza di lesione strutturale.
La disestesia da incretino-mimetici ha un profilo inconfondibile: compare rapidamente dopo l’aumento della dose, è quasi sempre lieve, e nella maggioranza dei casi si risolve spontaneamente nell’arco di settimane — anche senza interrompere il farmaco.
Incidenza attraverso gli studi: semaglutide, tirzepatide e oltre
Il gradiente dose-dipendente del semaglutide
Il dato più robusto disponibile viene dallo studio STEP UP, che per la prima volta ha confrontato sistematicamente due dosi di semaglutide con un terzo gruppo placebo. L’incidenza di eventi classificati come disestesia è stata dello 0,5% nel placebo, del 6,0% con semaglutide 2,4 mg e del 22,9% con semaglutide 7,2 mg (Wharton et al., 2025). Il rapporto di rischio relativo tra 7,2 mg e 2,4 mg è 3,84 (IC 95%: 2,23–6,72), e quello tra 7,2 mg e placebo è 46,05 (IC 95%: 8,26–261,45). Questi valori fotografano con precisione un effetto dose-dipendente molto netto: triplicando la dose il rischio di disestesia aumenta di quasi quattro volte rispetto alla dose inferiore.
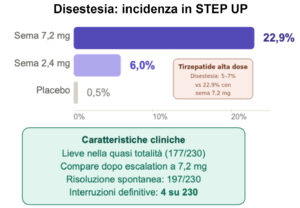
Il dato del 6,0% con semaglutide 2,4 mg merita attenzione perché, retroattivamente, suggerisce che la disestesia fosse già presente nei trial del programma STEP 1-10 ma non sistematicamente ricercata né uniformemente classificata. La disestesia era già nota con semaglutide 2,4 mg prima dello studio STEP UP. La bassa incidenza riportata nei trial precedenti riflette probabilmente una sottostima legata all’assenza di questa voce nei moduli di raccolta dati originali, corretta solo dopo i segnali emersi in corso di studio.
Tirzepatide e la classe più ampia
La disestesia non è un fenomeno esclusivo del semaglutide. Fenomeni di sensibilità cutanea alterata riconducibili alla disestesia sono stati documentati anche con tirzepatide nel programma di sviluppo clinico SURMOUNT. Nello studio di fase 2 su retatrutide — un agonista triplice dei recettori GIP, GLP-1 e glucagone attualmente in sviluppo — sono stati segnalati eventi di disestesia in tutti i gruppi di dosaggio attivo, con un’incidenza che aumentava alle dosi più alte (Jastreboff et al., 2023). Analogamente, lo studio OASIS 1 con semaglutide orale 50 mg ha documentato eventi di questa natura, seppur a incidenze inferiori rispetto alle dosi sottocutanee più alte (Knop et al., 2023).
Il quadro che emerge è quello di un effetto di classe degli incretino-mimetici, modulato dalla dose e probabilmente dall’entità dell’esposizione plasmatica al farmaco. Burke e colleghi, in una revisione delle implicazioni dermatologiche dei GLP-1 AR pubblicata nel 2025, sottolineano che la cute è un organo con elevata espressione di recettori GLP-1 e GIP, e che gli effetti cutanei di questi farmaci — non solo la disestesia, ma anche alterazioni delle ghiandole sebacee e delle unità pilosebacee — meritano un’attenzione sistematica che finora è mancata (Burke et al., 2025). [Revisione narrativa — non studio originale]
Quando compare e quando scompare: il pattern temporale
Il dato più clinicamente utile di STEP UP riguarda il timing della disestesia: la grande maggioranza degli eventi è insorta nelle settimane successive all’aumento della dose a 7,2 mg, avvenuto alla settimana 20. Questo è il primo elemento che distingue la disestesia da altri effetti collaterali della classe: gli eventi gastrointestinali si concentrano nelle fasi iniziali della titolazione, mentre la disestesia emerge dopo l’escalation verso la dose più alta (Wharton et al., 2025).
Dopo il picco iniziale, la prevalenza è diminuita nel corso delle settimane successive, anche in assenza di interruzione del farmaco. All’endpoint finale (settimana 72), la grande maggioranza dei partecipanti che avevano segnalato disestesia si era recuperata dall’evento: 197 su 230 nel gruppo 7,2 mg, 10 su 12 nel gruppo 2,4 mg e l’unico caso nel gruppo placebo. Quattro partecipanti nel gruppo 7,2 mg hanno interrotto definitivamente il trattamento per questo motivo; quarantasette hanno richiesto una riduzione temporanea della dose. Non sono stati registrati eventi gravi.
Il pattern — rapida comparsa, risoluzione tendenzialmente spontanea o con aggiustamento posologico, assenza di eventi gravi — è coerente con quanto descritto nel case report di Stokes e colleghi (2025), che documenta un caso di bruciore cutaneo da semaglutide risolto dopo riduzione della dose senza sequele, e con i dati preliminari di farmacovigilanza analizzati da Burke et al. (2025).
Meccanismo fisiopatologico: cosa sappiamo (e cosa non sappiamo)
Ipotesi neurogenica periferica
Il meccanismo alla base della disestesia da incretino-mimetici non è ancora chiarito. L’ipotesi più accreditata — e l’unica che gli autori di STEP UP ritengono compatibile con i dati — è una azione diretta del farmaco sui recettori neurali periferici. La cute esprime recettori GLP-1 non solo nelle strutture ghiandolari e nei cheratinociti, ma anche nelle terminazioni nervose sensoriali cutanee: fibre C amieliniche e fibre Aδ che trasmettono le sensazioni di dolore, temperatura e tatto (Burke et al., 2025). L’attivazione farmacologica di questi recettori a concentrazioni elevate potrebbe produrre un’eccitazione anomala delle terminazioni sensoriali, generando sensazioni di bruciore o ipersensibilità in assenza di stimoli lesivi.
A favore di questa ipotesi vi sono due evidenze indirette. La prima è la correlazione temporale con l’aumento della dose: la comparsa rapida degli eventi nella settimane successive all’escalation da 2,4 mg a 7,2 mg, e non nel corso dell’intera titolazione, indica che l’effetto è legato all’esposizione plasmatica al farmaco e non alla sua durata. La seconda è la dose-dipendenza coerente con un meccanismo recettoriale: l’incidenza quadruplica triplicando la dose, in modo compatibile con una curva concentrazione-effetto su recettori sensoriali.
Perché non è conseguenza della perdita di peso
L’altra ipotesi — che la disestesia sia un fenomeno secondario alle modificazioni della composizione corporea indotte dalla perdita di peso — appare improbabile alla luce dei dati temporali. Nelle settimane 16–20 la perdita di peso è già in atto in entrambi i gruppi attivi, ma la disestesia emerge in modo nettamente asimmetrico solo dopo l’aumento a 7,2 mg (Wharton et al., 2025). Inoltre, la disestesia è stata segnalata anche in studi come OASIS 1, in cui la formulazione orale del farmaco determina un’esposizione plasmatica di picco molto più alta rispetto alla formulazione sottocutanea a parità di effetto sulla perdita di peso (Knop et al., 2023), suggerendo che sia il profilo di esposizione — e non la variazione ponderale — a guidare il fenomeno.
Cosa manca ancora
Mancano studi di neurobiologia cutanea disegnati specificamente per questo effetto, biopsie cutanee in pazienti con disestesia attiva, e dati di farmacovigilanza sistematica che permettano di stimare l’incidenza reale in ambito clinico (fuori dai trial). L’effetto è inserito nel foglietto illustrativo di Wegovy e Zepbound, ma la sezione dedicata è ancora sintetica. Come osservano Burke et al. (2025), la dermatologia e la neurologia periferica sono discipline che fino ad oggi hanno avuto poco dialogo con l’endocrinologia metabolica: la disestesia da incretino-mimetici potrebbe essere uno dei punti di contatto che ne giustificherà uno in futuro.
Gestione clinica: cosa fare in pratica
La disestesia da GLP-1/GIP agonisti è un effetto collaterale nuovo per molti medici — e ancor più per i pazienti, che spesso non si aspettano sintomi cutanei da un farmaco per il controllo del peso. Una comunicazione preventiva, prima dell’aumento posologico, riduce l’impatto psicologico e migliora la gestione dell’evento quando si verifica.
L’algoritmo pratico che emerge dai dati di STEP UP è semplice:
- Evento lieve (bruciore o formicolio tollerabile, non interferisce con le attività quotidiane): proseguire alla dose attuale, informare il paziente che nella maggior parte dei casi il sintomo tende a diminuire nelle settimane successive all’escalation.
- Evento moderato (sintomatologia persistente e disturbante): valutare una riduzione temporanea della dose, con tentativo di rientro alla dose target dopo risoluzione. In STEP UP è stato esplicitamente raccomandato almeno un tentativo di recupero della dose prima di attestarsi permanentemente su un livello inferiore.
- Evento severo o persistente (interferisce significativamente con la qualità della vita e non migliora con la riduzione della dose): discutere con il paziente la sospensione del farmaco o il passaggio a un’altra terapia.
Non esistono al momento terapie farmacologiche specifiche per la disestesia da incretino-mimetici validate in trial. Le strategie empiriche derivate dalla gestione delle neuropatie periferiche da altre cause — emollienti, evitare tessuti sintetici o sfregamento, antiistaminici nei casi con componente pruriginosa prominente — possono offrire un sollievo sintomatico, ma non sono supportate da evidenze specifiche per questa indicazione. La priorità rimane la gestione della dose.
Conclusioni
La disestesia da incretino-mimetici è un effetto collaterale reale, dose-dipendente, legato alla classe farmacologica e non alla singola molecola. I dati di STEP UP lo documentano con la precisione di un trial randomizzato controllato; la letteratura dermatologica emergente lo contestualizza in un quadro biologico coerente. La natura nella maggior parte dei casi lieve, la tendenza alla risoluzione spontanea e la gestibilità con la modulazione della dose ne fanno un effetto collaterale rilevante ma raramente limitante.
La ricerca sul meccanismo è agli inizi: nei prossimi anni, la convergenza tra farmacologia degli incretino-mimetici e neurobiologia cutanea produrrà quasi certamente una comprensione più precisa — e probabilmente strategie di prevenzione o gestione specifiche. Nel frattempo, informare il paziente prima dell’aumento posologico e avere un piano di gestione pronto sono i due strumenti più efficaci a disposizione.
In sintesi: la disestesia da semaglutide, tirzepatide e altri GLP-1/GIP agonisti è un effetto collaterale di classe, dose-dipendente, tipicamente lieve e transitorio, che compare preferenzialmente nelle settimane successive all’escalation posologica e si risolve nella maggioranza dei casi con il solo monitoraggio o con una riduzione temporanea della dose; la comunicazione preventiva al paziente e una soglia bassa per l’aggiustamento posologico sono attualmente le principali misure di gestione clinica.
Domande frequenti
Ho iniziato a sentire bruciore alla pelle dopo l’ultima puntura di Wegovy. È normale?
La sensazione di bruciore cutaneo è un effetto collaterale riconosciuto del semaglutide, inserito nel foglietto illustrativo aggiornato. Nella maggior parte dei casi è lieve e tende a ridursi nelle settimane successive, anche senza modificare la dose. È importante segnalarlo al medico che segue la terapia, soprattutto se il sintomo è intenso, persistente o se è accompagnato da lesioni visibili sulla cute — in quel caso potrebbe trattarsi di qualcosa di diverso dalla disestesia da farmaco.
Tirzepatide (Mounjaro o Zepbound) dà gli stessi problemi?
Sì, la disestesia è stata segnalata anche con tirzepatide ed è riportata nel foglietto illustrativo statunitense di Zepbound. Tuttavia l’incidenza documentata nei trial SURMOUNT risulta inferiore rispetto a semaglutide 7,2 mg — la dose più alta di semaglutide sembra associata a una frequenza di disestesia più elevata rispetto a tirzepatide alle dosi approvate. Il fenomeno rimane un effetto di classe condiviso, ma l’entità dipende anche dalla molecola specifica e dalla dose.
Devo smettere il farmaco se compare la disestesia?
Nella grande maggioranza dei casi no. I dati di STEP UP mostrano che quasi tutti i partecipanti che hanno sviluppato disestesia si sono recuperati entro la fine dello studio, spesso senza interruzione del trattamento. Solo quattro partecipanti su 230 con disestesia nel gruppo semaglutide 7,2 mg hanno interrotto definitivamente il farmaco per questo motivo. Se il sintomo è tollerabile, il medico valuterà di mantenere la dose con monitoraggio; se è fastidioso, si può ridurre temporaneamente la dose con l’obiettivo di ritentare l’aumento in un secondo momento.
Perché compare sulla cute e non altrove?
La cute è un organo ricco di recettori GLP-1 e GIP, presenti sia nelle strutture ghiandolari sia — e questo è il punto rilevante — nelle terminazioni nervose sensoriali superficiali. L’ipotesi principale è che il farmaco, a concentrazioni elevate, attivi questi recettori nelle fibre nervose cutanee, producendo sensazioni anomale senza che vi sia un danno tissutale reale. Il meccanismo esatto è ancora oggetto di studio.
La disestesia può comparire anche con dosi basse, durante la titolazione?
Sì, ma con incidenza nettamente inferiore. In STEP UP il 6,0% dei partecipanti trattati con semaglutide 2,4 mg ha segnalato eventi di disestesia, contro il 22,9% con 7,2 mg. È plausibile che anche nei trial del programma STEP originale la disestesia fosse presente in percentuale simile, ma non fosse sistematicamente registrata per l’assenza della voce nei moduli di raccolta dati. In pratica, il rischio esiste a tutte le dosi terapeutiche, ma cresce significativamente con l’escalation.
Ci sono terapie specifiche per la disestesia da GLP-1 AR?
No. Al momento non esistono trattamenti farmacologici validati specificamente per questo effetto. La gestione si basa principalmente sull’aggiustamento della dose del farmaco incretino-mimetico. Alcune misure di supporto sintomatico — emollienti, indumenti di tessuto naturale morbido, evitare sfregamenti — possono alleviare il disagio, ma non sono supportate da evidenze specifiche per questa indicazione.
La disestesia è pericolosa a lungo termine?
Dai dati attualmente disponibili, no. In STEP UP non sono stati registrati eventi gravi né sequele neurologiche. La componente sensoriale si è risolta nella quasi totalità dei casi entro la fine dello studio. Mancano, tuttavia, dati di follow-up a lungo termine oltre le 72 settimane e studi di neurobiologia cutanea disegnati specificamente per questa domanda. Il monitoraggio prospettico dei pazienti trattati con dosi elevate di incretino-mimetici contribuirà a rispondere con maggiore certezza a questa domanda nei prossimi anni.
Glossario dei termini principali
Allodinia: dolore evocato da stimoli che normalmente non sono dolorosi, come il contatto con un tessuto o una leggera pressione. È una delle manifestazioni possibili della disestesia nei pazienti trattati con incretino-mimetici ad alta dose.
Disestesia: sensazione cutanea anomala e spiacevole — bruciore, formicolio, ipersensibilità, dolore superficiale — non associata a lesioni visibili della pelle. Nel contesto dei GLP-1 AR è un effetto collaterale di classe, dose-dipendente, con comparsa tipica nelle settimane successive all’aumento posologico.
Effetto di classe: effetto farmacologico — desiderato o indesiderato — condiviso da tutti i farmaci appartenenti allo stesso gruppo meccanicistico, indipendentemente dalle differenze strutturali tra le singole molecole. La disestesia sembra essere un effetto di classe degli incretino-mimetici che agiscono sul recettore GLP-1.
Fibre C e fibre Aδ: fibre nervose sensoriali periferiche responsabili della trasmissione di dolore, temperatura e sensazioni tattili fini. Le fibre C sono amieliniche (senza guaina isolante) e conducono lentamente; le fibre Aδ sono debolmente mielinizzate e più veloci. Entrambe esprimono recettori GLP-1 nelle terminazioni cutanee.
GIP (glucose-dependent insulinotropic polypeptide): ormone incretinico secreto dalle cellule K dell’intestino tenue in risposta all’assunzione di cibo. Amplifica la secrezione insulinica in modo glucosio-dipendente e agisce su numerosi tessuti extra-pancreatici, inclusa la cute. Il recettore GIP è il bersaglio aggiuntivo del tirzepatide rispetto al semaglutide.
GLP-1 AR (agonista del recettore GLP-1): classe di farmaci che mimano l’azione del GLP-1, ormone intestinale che riduce l’appetito, rallenta lo svuotamento gastrico e stimola la secrezione insulinica. Semaglutide (Wegovy, Ozempic) è un GLP-1 AR; tirzepatide (Mounjaro, Zepbound) agisce su GLP-1 e GIP simultaneamente.
Iperestesia: aumento abnorme della sensibilità a stimoli tattili normali. È una delle voci incluse nella categoria “disestesia” nei trial clinici sugli incretino-mimetici.
Parestesia: sensazione anomala di formicolio, intorpidimento o “pizzicore” non dolorosa, spesso descritta come “pelle che dorme”. Rientra nello spettro della disestesia.
Bibliografia
- Burke OM, et al. (2025)
- Dermatological implications of glucagon-like peptide-1 receptor agonist drugs. Skin Appendage Disord. 2025 Feb 14 [Epub ahead of print]. [Revisione narrativa — non studio originale]
https://doi.org/10.1159/000544023 - Jastreboff AM, et al. (2022)
- Tirzepatide once weekly for the treatment of obesity. N Engl J Med. 387:205–216.
https://doi.org/10.1056/NEJMoa2206038 - Jastreboff AM, et al. (2023)
- Retatrutide, a GIP, GLP-1 and glucagon receptor agonist, for people with obesity: a randomised, double-blind, placebo-controlled, phase 2 trial. N Engl J Med. 389:514–526.
https://doi.org/10.1056/NEJMoa2301972 [DOI da verificare prima della pubblicazione] - Knop FK, et al. (2023)
- Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 402:705–719.
doi: 10.1016/S0140-6736(23)01185-6. - Stokes ML, et al. (2025)
- A case of semaglutide-induced skin burning. Ann Intern Med Clin Cases. 4:e240568.
https://doi.org/10.7326/AIMCC.2024.0568 [DOI da verificare prima della pubblicazione] - Wharton S, et al. (2025)
- Once-weekly semaglutide 7.2 mg in adults with obesity (STEP UP): a randomised, controlled, phase 3b study. Lancet Diabetes Endocrinol. 2025 Sep 14 [Epub ahead of print].
https://doi.org/10.1016/S2213-8587(25)00226-8
